Autorom článku je Libor TRŠKO
Precipitácia je často sa vyskytujúci pojem najmä v oblasti vytvrdzovania hliníkových zliatin.V skutočnosti nachádza oveľa širšie uplatnenie pri spracovaní rôznych zliatin nielen za účelom zmeny ich mechanických ale aj ostatných fyzikálnych vlastností. V uvedenom článku je zhrnutá fyzikálna podstata, priebeh a využitie precipitačného vytvrdzovania.
Úvod
Presýtený tuhý roztok obsahuje rozpustené väčšie množstvo prísady ako je pre danú zliatinu pri danej teplote termodynamicky výhodné. Takýto tuhý roztok sa prirodzene snažío dosiahnutie stavu s najnižšou voľnou entalpiou a rozpadá sa. Tento rozpad prebieha najčastejšie heterogénnou fázovou premenou, ktorá sa nazýva precipitácia. Menej často (napr. v sústavách Al-Zn alebo Cu-Ni-Fe) sa uskutočňuje homogénnou fázovou premenou,tzv. spinodálnym rozpadom. Pod pojmom segregácia (na rozdiel od precipitácie) sa obvykle rozumie iba vznik heterogenity chemického zloženia, bez vzniku novej fázy (hovoríme preto o precipitácii fázy a segregácii prvku) [1].
Pri precipitáci z presýteného tuhého roztoku sa menia mechanické a fyzikálne vlastnosti materiálu. Štruktúrne citlivé vlastnosti ako tvrdosť, medza sklzu, ťažnosť,kontrakcia,odolnosť proti korózii a pod. sú mimoriadne závislé na rozložení jednotlivých fáz v štruktúre. Počiatočné štádiá precipitácie spôsobujú najväčšie vytvrdenie. Po dosiahnutíkritickej veľkosti precipitátov v precipitačne spevnených zliatinách, dochádza k zníženiu hodnôt medze sklzu (Re, Rpo,2), medze pevnosti (Rm)resp. tvrdosti. Precipitácia môže ovplyvňovať vlastnosti materiálu aj nežiaducim spôsobom, napr. vznik popúšťacej krehkosti,štruktúrna nestabilita pri creepe a pod [1].
Podstata a mechanizmus
Podmienkou pre rozpad presýteného tuhého roztoku a vznik precipitujúcej fázy je zníženie rozpustnosti jedného, alebo viacerých prvkov v tuhom roztoku pri zmene vonkajších podmienok,obvykle pri znížení teploty [1]. K precipitácii teda môže dôjsť iba v zliatinách,ktorých rovnovážne diagramy spĺňajú nasledujúce podmienky:
– výrazné maximum rozpustnosti jednej zložky v druhej v závislosti od jej obsahu,
– klesajúca rozpustnosť so znižujúcu sa teplotou [2].
Na Obr.1 je zobrazený rovnovážny binárny diagram spĺňajúci podmienky pre precipitáciu,pričom z1 predstavuje čiaru koncentrácie precipitačne vytvrditeľnej zliatiny a na jej príklade budú popisované jednotlivé procesy prebiehajúce pri jej tuhnutí a následnom vytvrdzovaní.
Pri plynulom ochladzovaní v bode 1 vzniknú v tavenine prvé kryštály tuhého roztoku a. V bode 2 je kryštalizácia ukončená a štruktúru tvorí iba tuhý roztok a. V bode 3 začne klesat rozpustnosť zložky B v tomto tuhom roztoku. Keďže ochladzovanie prebieha v rovnovážnych podmienkach je dostatok času pre difúziu a nadbytočná zložka B sa vylúči po hraniciach zŕn ako intermediárna fáza AmBn.
Ak materiál prudko ochladíme z teploty, ktorá sa nachádza medzi bodmi 2 a 3, potlačíme tým difúziu a výsledný tuhý roztok (a‘) bude termodynamicky nestabilný (metastabilný)a preto sa rozpadá samovoľ’ne pri teplote okolia (prirodzené starnutie) alebo pri zvýšenej teplote (umelé starnutie).
Na defektoch mriežky vznikajú zárodky precipitujúcej fázy AmBn(koncentrácia jednotlivých zložiek zodpovedá stechiometrickému pomeru danej intermediárnej fázy). Na fázovom rozhraní medzi AmBn a a‘ sa koncentrácia B mení skokom na koncentráciu blízku rovnovážnej. V dostatočnej vzdialenosti od častice má fáza a‘ stále koncentráciu zodpovedajúcu zliatine z1. K ďalšiemu rastu častice (Obr. 2) je nutný difúzny pohyb prvku B na zväčšujúcu sa vzdialenosť a koncentračný gradient vo fáze a‘ preto postupne klesá. V čase t = ao je dosiahnutá termodynamická rovnováha a tuhý roztok a má vo všetkých miestach rovnovážnu koncentráciu [1].
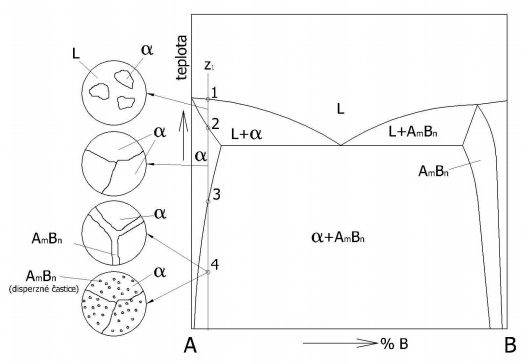
Obr.1 Binárny rovnovážny diagram ktorý spĺňa podmienky pre precipitáciu [1][2].
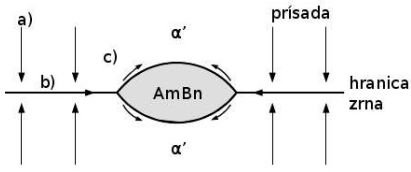
Obr. 2 Difúzny rast precipitátu na hranici zrna a) objemová difúzia prísady B cez zrno k jeho hranici, b) difúzia prísady B pozdĺž hranice zŕn a‘- a‘, c) difúzia prísady B pozdĺžmedzifázového rozhrania a‘-AmBn, ktorá umožňuje rýchle hrubnutie častice [3].
Štádiá precipitácie
Precipičaný proces má vo všeobecnosti tri štádiá: najskôr sa vytvárajú v presýtenom tuhom roztoku segregované oblasti s pravidelným rozdelením atómov v mriežke tzv. Guinierove -Prestonove zóny, potom sa vylučuje prechodový precipitát a nakoniec rovnovážny precipitát,ktorý je s matricou nekoherentný (Obr. 3). Počet prechodových stavov precipitátov sa môže v jednotlivých zliatinách odlišovať. Najväčší počet prechodových stavov má sústava Al-Cu a je taktiež najdôkladnejšie preštudovaná [1].
Guinierove- Prestonove zóny (GPZ) – sú oblasťami zvýšenej koncentrácie intermediárnej fázy v tuhom roztoku. V prípade, keď sú atómové priemery zložiek rozdielne,GPZ majú inýmriežkový parameter ako miesta chudobnejšie na danú zložku. Nakoľko sú GPZ koherentnés tuhým roztokom (nie sú oddelené medzifázovou hranicou), vytvárajú mriežkové napätia,ktoré zvyšujú tvrdosť a pevnosť materiálu [2].
Prechodový semikoherentný precipitát- koncentrácia B dosahuje v zónach približne stechiometrický pomer AmBn a tým nastáva preskupenie iónov v týchto zónach [2].
Rovnovážny precipitát- dôjde k úplnému preskupeniu atómov na iný typ mriežky. Stráca sa koherencia a vytvrdenie napätovými poľami sa mení na typické precipitačné vytvrdenie ktorého efekt je o niečo nižší [2].
a) Rozpúštany atóm(A) atóm(B)

b) GPZ koherentné s mriežkou tuhého roztoku
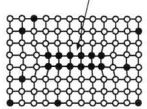
c) semikoherentný precipitát
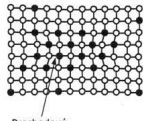
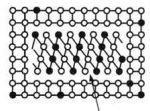
d) rovnovážny precipitát
Obr. 3 Schéma štádií starnutia: a) presýtený tuhý roztok,b) Guinierove – Prestonove zóny,c) prechodový precipitát, d) rovnovážny precipitát[2].
Termodynamika precipitácie
Príčinou a hnacím mechanizmom vzniku precipitátov je snaha o dosiahnutie čo najnižšej voľnej entalpie sústavy. Vznik jednotlivých štádií precipitácie vyplýva z rozboru koncentračných závislostí voľnej entalpie fáz a, AAmBnBn a β. Obr. 4 znázorňuje takýto rozbor pre teplotu T1 na Obr.1.
V rovnovážnom stave zliatiny s koncentráciou co a voľnou entalpiou Go, je sústava tvorenáfázou a s koncentráciou c, a voľ’nou entalpiou G1 a fázou AmBn s koncentráciou C2 a voľ’nou entalpiou G2. Podľ’a pákového pravidla platí:
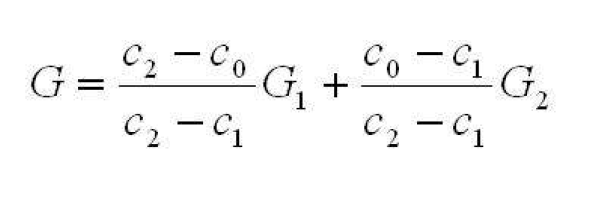
Po rýchlom ochladení je sústava tvorená iba presýteným tuhým roztokom fázy a‘ a je charakterizovaná voľ’nou entalpiou G’o- Akákoľvek zmena v sústave je možná len keď bude jej voľná entalpia klesať (G’o→ V presýtenej matrici a‘ bude ubúdať množstvo prvku B, takže co→c, bude prebiehať po krivke o’o” 1. Vylúčením malého podielu precipitujúcej fázy sa zloženie fázy a‘ posunie napr. do bodu o”. Vznik izomorfnej precipitujúcej fázy napr. so zložením o” nie je pri danom priebehu Ga možný, pretože by voľná entalpia sústavy vzrástla ”).Preto zloženie precipitujúcej fázy bude ležať na dotyčnici ku krivke Ga prechádzajúcou bodom o”. Uvažujú sa fázyAmBn(s hodnotami c2 a G2)a fázy β(s hodnotami c3 a G3). Priesečník dotyčnice prechádzajúci bodom o”s koncentráciou C3 udáva voľnú entalpiu G’3, ktorú možno analogicky vypočítať podľa vzťahu (1). Hodnota G’3 je súčtom voľnej entalpie G3 fázy β a hybnej sily ΔG3 pre precipitáciu danej fázy. Obdobné úvahy platia aj pre precipitujúcu fázu AmBn, ktorá má síce nižšiu voľnú entalpiu G2 než je G3,takže by jej vznikom voľná entalpia sústavy poklesla viacej, ale ktorá má aj menšiu hybnú silu ΔG2<G3pre svoj vznik. Preto najskôr precipituje prechodná fáza B a neskôr rovnovážna fáza AmBn [1].
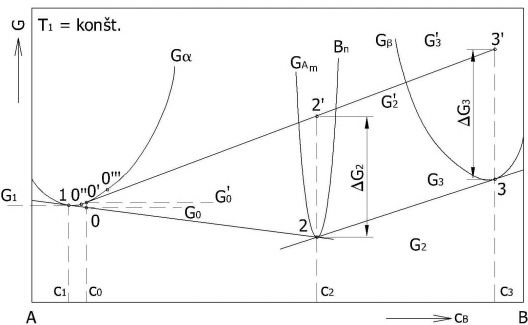
Obr. 4 Koncentračná závislosť voľnej entalpie G fáz a, AmBn a β pri teplote T1 zodpovedajúcej rovnovážnemu diagramu na Obr.1 [1].
Praktický význam precipitácie
Rozpad presýteného tuhého roztoku je možné cielene využívať na zmenu mechanických vlastností požadovaným smerom. Existuje množstvo systémov, ktoré vyhovujú podmienkam pre vznik precipitácie, avšak prakticky sa zatiaľ‘ využívajú iba niektoré.
Vytvrditelné zliatiny Al obsahujú ako vytvrdzovacie prvky najčastejšie Cu alebo Mg (prípadne oba prvky súčasne).
Zliatiny typu AlCu4Mgsa nazývajú duraly, so zvýšeným obsahom horčíka (AlCu4Mg1) superduraly. Najčastejšie sa vytvrdzujú za podmienok 495 až 515 °℃/voda/20 °℃, 4 h na Rm = 400 MPa u duralu alebo 450 MPa u superduralu. Zmeny mechanických vlastností pri starnutí superduralu (viď‘ Obr. 5) naznačujú, že maximálne zvýšenie Rpo,2 možno dosiahnuť len umelým starnutím, ale vedie to k rýchlemu poklesu ťažnosti i odolnosti proti korózii[4].
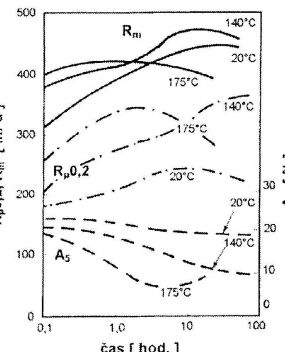
Obr. 5. závislosť mechanických vlastností zliatiny AlCu4Mg1 od doby a teploty starnutia [4].
Zliatiny Al-Mg-Sisa nazývajú avialy. Sú to vytvrditeľné zliatiny pre tvárnenie,charakteristické nižšou pevnosťou, ale vyššou koróznou odolnostou a vyššou húževnatosťou v porovnaní s duralmi. Ich vytvrditeľ’nosť je podmienená precipitáciou fázy Mg2Si. Rozpad presýteného tuhého roztoku apres sa uskutočňuje podľa schémy: apres →GPI→GPII →β'(fáza so stechiometrickým pomerom blízkym Mg2Si)→β(Mg2Si).
Priemyselné zliatiny je možné rozdeliť do dvoch skupín:
a) Zliatiny s prebytkom Mg. V dôsledku väčšieho množstva Mg, aké je potrebnék vytvoreniu príslušného množstva Mg2Si sa zvyšuje odolnosť voči korózii, znižujú sa pevnostné vlastnosti a zhoršuje sa tvárniteľnosť v porovnaní so zliatinami, kde je rovnakémnožstvo intermetalickej fázy Mg2Si, ale bez prebytku Mg.
b) Zliatiny s prebytkom Si. V dôsledku prebytku Si sa zvyšujú pevnostné vlastnosti zliatiny,bez zníženia schopnosti k tvárneniu a bez zhoršenia zvariteľnosti. Čiastočne sa znižuje odolnosť‘ týchto zliatin voči interkryštalickej korózii.
Avialy sa v stave vytvrdenom za tepla (520 až 535 °℃/voda/160 C,5h) bežne spevňujú tvárnením za studena na Rm=400 MPa. Naopak zníženie pevnosti a tvrdosti zliatiny jeRm=400možné dosiahnuť žíhaním (340 až 370 °℃) a pomalým ochladením(max.100°C.h-1)[4].
Vytvrdzovanie žiaruevných zliatin Ni. Žiarupevné zliatiny niklu sú založené na báze tuhého roztoku Ni s prísadovými prvkami Al a Ti, prípadne Cr tvoriace hlavnú vytvrdzujúcu fázu. Vytvrdzovanie žiarupevných zliatin niklu je ich najnáročnejším tepelným spracovaním. Snahou je dosiahnuť optimálnu kombináciu množstva, tvaru, veľkosti a spôsobu vylúčenia spevňujúcej fázy v objeme zliatiny. Ti tvorí intermetalickú fázu Ni3Ti,hliník Ni3Al. V prípade, že sú v zliatine oba prvky, vzniká fáza Ni3(Ti,Al), ktorú možno považovať za tuhý roztok titánu v intermetalickej fáze Ni,Al. Označuje sa symbolom y'[5].
Teplota rozpúšťacieho žíhania musí byť dostatočne vysoká pre čo najúplnejšie rozpustenie fázy y‘. V závislosti na chemickom zložení zliatiny býva v rozmedzí 1080 ℃ až 1320 ℃.Ohrev trvá od 2 h do 12 h a realizuje sa vo vákuových peciach alebo v peciach s ochrannou atmosférou aby sa zamedzilo ochudobňovaniu povrchu súčiastky o legujúce prvky, prípadne jej oxidácii. Ochladzovanie z teploty rozpúšťacieho žíhania sa realizuje obyčajne na vzduchu.Prudké ochladenie vo vode vedie k vzniku trhlín a to najmä vo vysokolegovaných zliatinách s nízkou húževnatostou [5].
Starnutie zliatin prebieha pri ohreve na teplotu vyššiu než je prevádzková teplota súčiastky.Teploty starnutia sa pohybujú od 700 do 1150 ℃. Pri starnutí sa z presýteného tuhého roztoku vylučujú precipitáty fázy y‘ a prípadne karbidy, ak sa medzi legujúcimi prvkami nachádza C. U niektorých zliatin prebieha vytvrdzovanie takzvaným viacstupňovým starnutím, pri ktorom sa dosiahne výhodnejšie vylúčenie y‘ fázy.Takto vytvrdené zliatiny dosahujú postačujúcu dlhodobú žiarupevnosť pri najvyšších pracovných teplotách [5].
Z velkého množstva prakticky využívaných vytvrditeľných zliatin boli uvedené len tie najzákladnejšie. Mnoho ďalších zliatin sa ešte len vyvíja za účelom nahradenia niektorých komerčne využívaných materiálov, ktoré niektorým parametrom úplne nevyhovujú pre danú funkciu (napr. vysoká hmotnosť, nízka korózna odolnosť, nízka žiarupevnost)a umožnia tak vyššiu bezpečnosť a lepšiu optimalizáciu súčiastok.